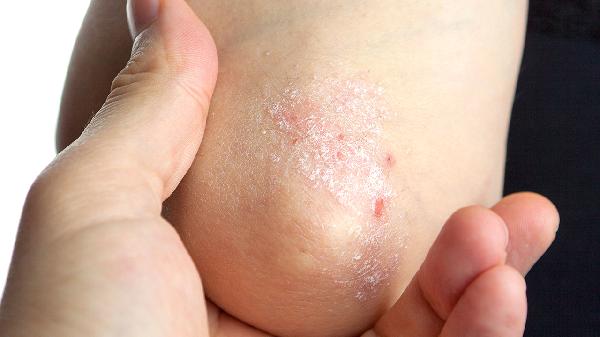
2024年11月,由上海泽德曼医药科技有限公司研发的中国原研创新药泽立美®本维莫德乳膏正式获得国家药品监督管理局(NMPA)批准上市,成为全球首个用于2岁及以上儿童与成人特应性皮炎(AD)治疗的芳香烃受体(AhR)调节剂。仅20天后,该药又获美国食品药品监督管理局(FDA)批准上市。这一突破性成果,标志着本维莫德继2019年在全球率先获批银屑病适应症后,再次以“中国智慧”重塑AD治疗格局。
尤为值得关注的是,从NMPA优先审评到FDA快速跟进仅间隔20天,充分体现了我国监管科学水平的提升和国际认可度的增强,也彰显了中国新药研发已实现从“跟随模仿”向“原创引领”的历史性跨越。
近日,北京大学人民医院张建中教授团队在国际权威期刊《Chinese Medical Journal》(IF=7.3)发表的Ⅲ期临床研究——《Efficacy and safety of benvitimod 1% cream for atopic dermatitis in patients aged 2 years and older: A phase III randomized clinical trial》[1]——以严谨的循证数据证实:泽立美®本维莫德乳膏(benvitimod)对2岁及以上儿童及成人AD具有显著疗效与良好安全性。该研究进一步揭示,泽立美®本维莫德乳膏不仅起效迅速、疗效持久,且缓解期长、复发率低,长期安全性好,展现出卓越的长期管理潜力。且目前在儿童AD患者中缺少疗效好、安全性优的外用药,泽立美®本维莫德乳膏为成人及儿童AD患者提供了更优的治疗选择。

功能主治:本品用于适合局部治疗的成人轻至中度稳定性寻常型银屑病
用法用量:皮肤局部外用,每日两次,早晚各一次,均匀涂抹于患处,形成一薄层即可。 每日最大使用剂量不超过6g,治疗面积不应超过体表面积的10%。患处皮肤涂布本品后严禁日光照射,在自然光照下也需注意采取避光措施。本品连续使用超过12周的安全有效性尚未确立。临床用药总时间最长不得超过12周。本品停药后重复使用的安全有效性尚未确立,不推荐重复使用。本品不可用于头面部、口周及眼睑部、腹股沟、肛门生殖器等部位。用药后请立即洗手。
该研究第一作者为来自北京大学人民医院赵琰教授,北京大学人民医院张建中教授为通讯作者。该突破性研究不仅为全球AD患者提供了新的治疗选择,更以“双适应症全球首批”的里程碑事件,奠定了中国在全球医药创新浪潮中的引领地位。
研究背景
AD是一种全球范围内高发的慢性、复发性炎症性皮肤病,全球约2%~10%成人和15%~30%儿童受其困扰,不仅带来剧烈瘙痒与皮肤损伤,更对患者的心理健康、睡眠质量及整体生活质量造成深远影响。其病理机制复杂,涉及皮肤屏障功能障碍、异常免疫激活(尤其是Th2型炎症)以及皮肤微生物群紊乱,传统治疗如外用糖皮质激素虽具疗效,但长期使用存在皮肤萎缩、色素沉着等副作用风险,限制了其在中重度患者中的长期应用。
近年来,靶向AhR的新型非甾体药物本维莫德脱颖而出——通过激活AhR通路,同时修复表皮屏障、调节氧化应激与抗炎信号,实现多维度干预。2019年,本维莫德在中国获批用于银屑病局部治疗,并于2022年获美国FDA批准。本研究报道了泽立美®本维莫德乳膏治疗成人与儿童中重度AD患者的Ⅲ期临床试验结果。为这一亟须创新疗法的患者提供了科学依据与临床新选择。
研究方法
该研究是一项多中心、随机、双盲、安慰剂对照的Ⅲ期临床试验,旨在评估泽立美®本维莫德乳膏在成人与儿童中重度AD患者中的疗效与安全性。研究于2023年6月至11月在中国35个研究中心开展,采用分层区组随机化方法(按IGA评分[3 vs. 4]和年龄组[2–6岁、7–11岁、12–17岁、≥18岁]分层),以2:1比例分配受试者至泽立美®本维莫德乳膏组或安慰剂对照组,确保组间均衡。
入选标准包括:年龄≥2岁、中国患者、病程符合年龄分层要求(2-11岁至少3个月,12-17岁至少6个月,成人≥1年),且基线IGA评分≥3、体表受累面积(BSA)为5%–35%(不包括头皮)。
治疗为期8周,每日早晚外用泽立美®本维莫德乳膏或安慰剂(安慰剂为本维莫德乳膏的润肤基质,不含活性成分);结束后可进入44周开放标签扩展期,持续使用泽立美®本维莫德乳膏直至IGA评分降至0。双盲阶段允许使用温和保湿剂,扩展期可短期使用局部钙调磷酸酶抑制剂作为挽救治疗(图1)。主要终点为第8周EASI改善≥75%的患者比例,关键次要终点为达到IGA 0/1且较基线下降≥2分的患者比例,其他次要终点包括EASI 90、BSA变化及瘙痒评分(PP-NRS)降低≥3分的比例。
安全性方面,通过不良事件(TEAEs)、严重不良事件、局部反应、实验室检查及心电图等多维度评估。整个研究流程标准化、数据质量可控,为泽立美®本维莫德乳膏在不同年龄段AD患者中的应用提供了高质量循证依据。
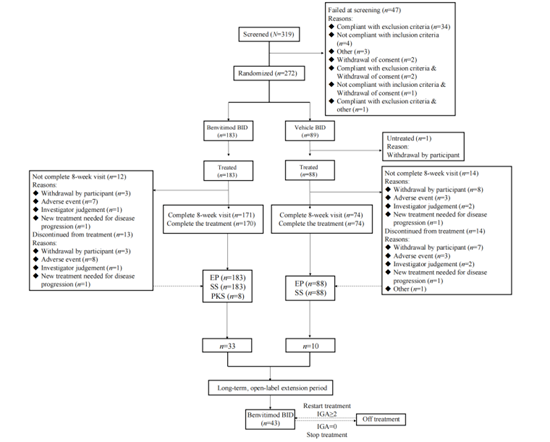
图1:CONSORT患者分组流程图
研究结果
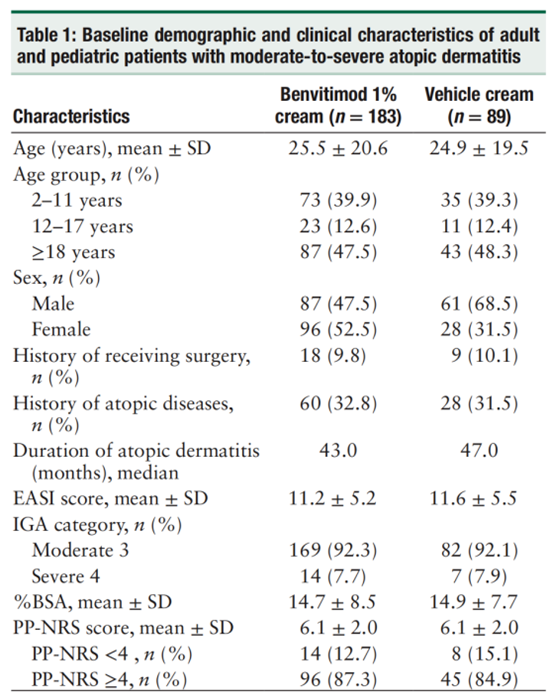
本研究共纳入272例中重度AD患者,其中183例接受泽立美®本维莫德乳膏治疗,89例接受安慰剂对照。两组在基线人口学特征和基线疾病特征平衡(表1),且泽立美®本维莫德乳膏组的脱落率显著低于对照组(7.1% vs. 15.9%),提示其良好的依从性和耐受性。
表1:基线人口学特征及临床特征
治疗第8周时,泽立美®本维莫德乳膏组EASI 75应答率显著高于对照组(54.4% vs 25.5%,Δ28.9%,P<0.001)(图2),这一优势早在第1周即显现(数值差异12.3%),至第4周达统计学意义(37.9% vs 19.7%,P=0.007)。更值得注意的是,儿童亚组(2-17岁)疗效更为突出,EASI 75应答率达69.2%(vs 31.0%,Δ38.2%)(表2)。说明泽立美®本维莫德乳膏对不同年龄段人群均具有强效作用。
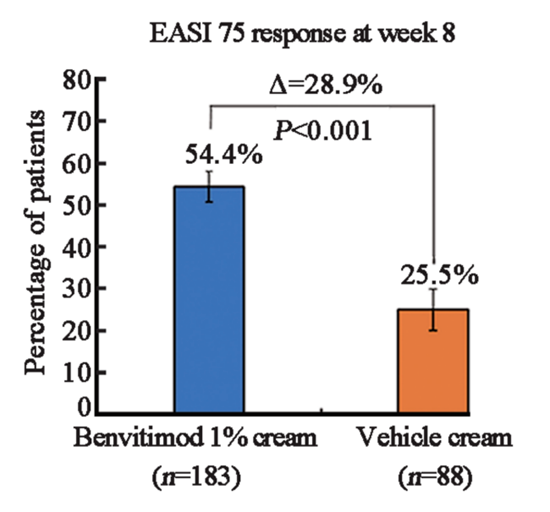
图2:第8周达到EASI 75的患者比例
表2:基于年龄分层的亚组疗效分析
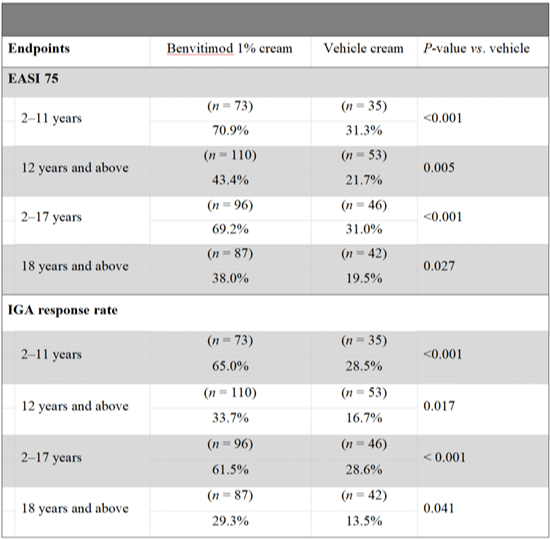
此外,第8周时,泽立美®本维莫德乳膏组IGA评分达到0/1的患者比例为46.2%,也显著优于对照组的21.4%(Δ24.9%,P<0.001)(图3)。EASI 90应答率分别为33.9%和13.5%(P<0.001);BSA平均减少幅度也明显更大。在≥12岁患者中,瘙痒症状显著缓解——泽立美®本维莫德乳膏组有54.0%(n=47)的患者实现PP-NRS评分下降≥3分,而对照组仅为27.9%(n=12;P=0.005),进一步验证了泽立美®本维莫德乳膏对症状控制和生活质量的改善价值(图4)。
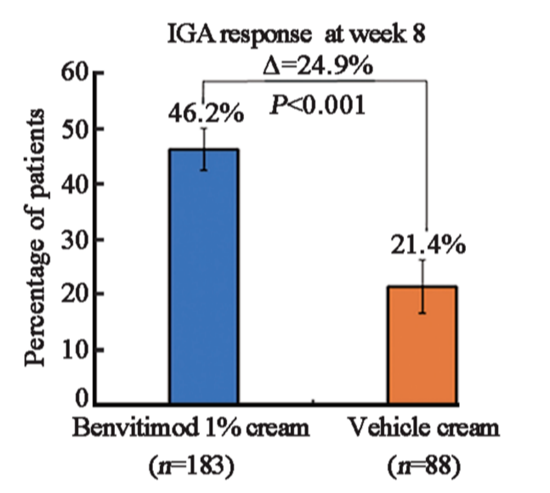
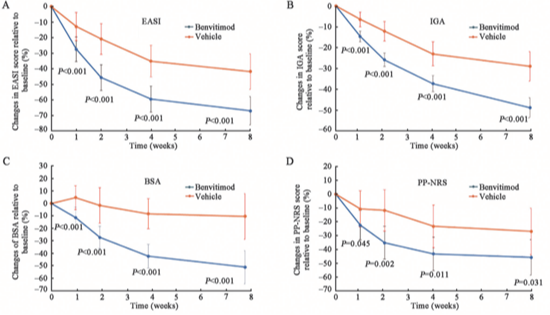
图4:各临床指标在8周治疗期的纵向变化趋势
安全性方面,泽立美®本维莫德组治疗相关不良事件(TEAEs)发生率为51.4%,安慰剂组为43.2%,多数为轻至中度,主要为用药部位反应(8.7% vs 1.1%)和毛囊炎(7.7% vs 4.5%)。3-5级TEAEs罕见,分别为4.4%和3.4%。无死亡事件报告,且因不良事件导致的停药率相近(4.4% vs. 3.4%),显示出良好的整体安全性。
在开放标签扩展阶段,43名来自原始研究队列的患者继续接受本维莫德乳膏治疗,其中27例(62.7%)的患者至少一次达到并维持IGA =0/1状态超过16周,表明该药物不仅具有显著短期疗效,还能在较长时间内维持临床改善。Kaplan-Meier分析显示,在18例达到IGA 0的开放标签应答者中,无复发率在约200天时逐渐下降至约50%,随后在一年随访期内趋于平稳(图5)。整个开放标签阶段仅报告一例3级治疗期间出现的不良事件(代谢综合征),未发现其他3-5级严重不良事件。
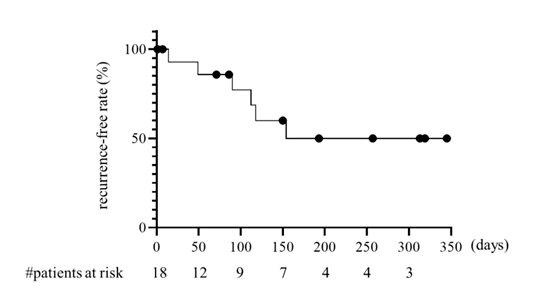
图5:达到IGA 0的开放标签应答者的Kaplan-Meier复发时间曲线
研究讨论
本Ⅲ期临床研究进一步证实,泽立美®本维莫德乳膏在成人与儿童中重度AD患者中展现出卓越且持久的疗效,与ADORING和ZBB4等国际多中心研究结果相互印证,且无论每日一次还是两次给药方案,泽立美®本维莫德乳膏均能在8周内显著改善皮损、整体疾病严重程度及瘙痒症状,在不同人群、地域和给药频率下保持高度一致性,凸显其强大的抗炎作用和广泛的临床适用性。
开放标签延展期数据显示,多数患者在持续使用泽立美®本维莫德乳膏后能维持IGA 0/1状态,甚至部分患者在停药后仍保持长期缓解,这一现象与银屑病领域观察到的“停药后持续获益”相似,提示泽立美®本维莫德乳膏可能通过重塑皮肤免疫稳态实现长期疗效,而非单纯依赖持续用药。尽管当前数据来自小样本自愿延伸人群,其探索价值不容忽视,为未来制定个体化维持治疗策略提供了重要参考。
泽立美®本维莫德乳膏通过靶向AhR发挥多重免疫调节作用,其机制已获关键实验证实。AhR通路不仅修复皮肤屏障,还可调控角质形成细胞、T淋巴细胞(如Th17、γδ T细胞)、先天淋巴样细胞(ILC3)及神经元等多种细胞类型,从而全面抑制炎症、恢复皮肤稳态。这些发现表明,靶向AhR为特应性皮炎提供了一种多维度、机制清晰的治疗策略。综上所述,泽立美®本维莫德乳膏不仅具备快速起效、疗效持久、安全性良好三大优势,更因其独特的分子机制展现出成为AD外用治疗新选择的巨大潜力。
总结:中国新药的标杆,引领世界的旗帜
如今,中国创新药正稳步迈向国际舞台,泽立美®本维莫德乳膏的突破性进展正是这一进程中的重要里程碑。这项研究的背后,是科研团队对临床需求的细致回应与对科学路径的持续探索。从实验室到病房,从本土获批到全球认可,泽立美®本维莫德乳膏的成功标志着中国医药创新已从“跟跑”迈向“并跑”甚至“领跑”,为全球患者带来希望的同时,也树立起中国智慧在全球健康治理中的新标杆。

张建中
北京大学人民医院皮肤科
主任医师 教授 博士生导师 国家名医
中华医学会皮肤性病学分会第13届主任委员
中国康复医学会皮肤病康复专委会名誉主任委员
全球华人医师协会皮肤科医师分会副会长
中国毛发研究会(CHRS)主席
皇家爱丁堡医师学会会员
美国皮肤科学会(AAD)国际会员
JAAD 编委
研究领域:特应性皮炎、银屑病、脱发等
2023年中国Leading PI前20,2024年中国Leading PI前3
参考文献:
[1]Zhao Y, Wei Z, Feng Y, Ma L, Jiao D, Cui Y, Gu J, Bian K, Ci C, Zhu J, Lei T, Shi Y, Tao X, Han X, Zhang X, Zhang L, Li Y, Chen G, Zhang J; study group. Efficacy and safety of benvitimod 1% cream for atopic dermatitis in patients aged 2 years and older: A phase Ⅲ randomized clinical trial. Chin Med J (Engl). 2025 Sep 16. doi: 10.1097/CM9.0000000000003769. Epub ahead of print. PMID: 40960153.