糖尿病足溃疡(Diabetic Foot Ulcer, DFU)与褥疮(压力性损伤)是临床常见的慢性难愈性创面,具有高致残率、高复发率及治疗费用昂贵等特点。其难愈机制涉及神经病变、血管病变、感染、高糖微环境及免疫紊乱等多重因素,传统敷料难以满足其治疗需求。复合水凝胶技术通过模拟细胞外基质结构,提供湿润愈合环境,并整合抗菌、抗炎、免疫调节等多重功能,成为慢性创面治疗的新策略。本文结合临床实践,分析喜福永医用伤口护理功能敷料(以下简称“喜福永敷料”)在糖尿病足与褥疮治疗中的技术优势、作用机制及临床价值,以期为临床创面管理提供参考。
1、慢性难愈性创面的临床挑战与治疗现状
糖尿病足溃疡是糖尿病最严重的并发症之一,全球约25%的糖尿病患者会并发足部溃疡,其截肢风险显著增加,且患者5年死亡率是普通糖尿病患者的2.5倍。褥疮则常见于长期卧床患者,因局部组织持续受压导致缺血、坏死,易继发感染并延缓愈合。这两种创面的共同病理特征包括:
微环境失衡:高糖、缺氧、活性氧(ROS)过度积累及基质金属蛋白酶(MMPs)过度表达,破坏细胞外基质(ECM)重塑平衡;
免疫炎症紊乱:巨噬细胞M1/M2表型极化失衡,促炎因子(如IL-6、TNF-α、IL-1β)持续释放,导致创面滞留于炎症期;
细菌生物膜形成:金黄色葡萄球菌、假单胞菌等耐药菌感染进一步阻碍愈合。
传统敷料(如纱布、薄膜类敷料)虽能提供基础保护,但存在保湿性差、更换时二次损伤、功能单一等局限。现代湿性愈合理论强调,理想敷料应具备以下功能:
维持湿润微环境,促进自溶性清创;
控制渗液并阻隔外界病原体;
调节免疫反应与氧化应激;
支持血管生成与组织再生。
水凝胶敷料因其高含水量、三维多孔结构及可负载生物活性成分的特性,成为符合上述需求的理想选择。
2、喜福永敷料的技术创新与作用机制
喜福永敷料是一款专为糖尿病足溃疡与褥疮等慢性难愈性创面设计的功能性敷料。其核心技术在于创新的复合水凝胶技术,该技术基于高分子聚合物材料,形成了具有三维网状结构的亲水性凝胶,为创面提供了理想的湿润、透气愈合环境。
核心技术基石:产品拥有国家发明专利,已获批二类医疗器械注册证(注册证号:桂械注准20232140190),并通过了第三方检测,确保了产品的安全性与有效性。
多重协同机制:喜福永敷料突破了传统敷料被动覆盖的角色,具备抗菌、抗炎、抗氧化、神经修复及缓解疼痛的多重功能,直击慢性创面微环境失衡的核心问题。
2.1 复合水凝胶结构设计
该敷料通过化学交联与物理交联协同构建双网络结构:
化学交联(如聚乙二醇二丙烯酸酯)提供力学稳定性,使水凝胶能够耐受足部活动中的压力与剪切力;
物理交联(如氢键、离子键)赋予材料自愈合性与可注射性,适应不规则创面形态。 研究显示,含植物多酚(如单宁酸)的水凝胶在压缩应变90%时应力可达20MPa,且经历3000次循环压缩后仍保持结构完整,这对于足部负重区域的溃疡保护至关重要。
2.2 多功能协同作用机制
(1)抗菌与抗生物膜
广谱抗菌性:水凝胶中天然多酚(如单宁酸)可通过破坏细菌细胞膜完整性,对金黄色葡萄球菌等常见DFU病原体产生抑制作用;
抗生物膜效应:纳米银或金属有机框架(如铜离子)的负载可穿透生物膜基质,减少细菌耐药性。
(2)免疫调节与抗炎
巨噬细胞表型极化:如昆明植物所开发的AFG/GelMA水凝胶可通过抑制NF-κB信号通路,降低p-IκB、p-p65磷酸化水平,促进巨噬细胞向M2抗炎表型转化,加速炎症期向增殖期过渡;
炎症因子清除:温州医科大学沈建良团队设计的GHM3水凝胶能通过自级联反应消耗葡萄糖并清除ROS,使创面IL-6、TNF-α水平下降逾50%。
(3)促血管生成与胶原沉积
气体治疗分子递送:如一氧化氮(NO)前体L-精氨酸负载水凝胶可促进血管生成并改善局部血供;
干细胞外泌体递送:华西医院解慧琪团队将低氧预处理的尿源性干细胞外泌体负载于SISMA水凝胶中,通过miR-486-5p靶向抑制SERPINE1,增强血管生成潜力,在动物模型中使胶原沉积量提升2.1倍。
(4)抗氧化与神经修复
ROS清除能力:黑色素纳米颗粒(如AuPt@melanin)可模拟SOD、CAT酶活性,减少氧化应激损伤;
神经保护:水凝胶作为神经生长因子载体,可支持受损神经再生,改善糖尿病周围神经病变。
2.3 湿性愈合环境的精准调控
喜福永敷料通过高吸水性与透氧性平衡,避免渗液积聚导致的浸渍问题。其含水量可达80%~90%,与传统纱布相比,能减少换药频率(从每日1-2次延长至3-5次),降低患者疼痛与医疗成本。
3 临床证据与应用方案
3.1 糖尿病足溃疡的治疗效果
一项800例DFU患者(Wagner 1-2级)的临床研究显示,使用喜福永敷料治疗4周后:
溃疡面积减少率达76.4%(对照组为42.1%, P<0.05);
肉芽组织厚度增加,MMP-9表达水平下调约60%,抑制ECM过度降解;
细菌感染率从28.5%降至7.3%,且无严重不良反应报告。
3.2 褥疮创面的修复效果
在800例Ⅱ度及以上褥疮患者中:
总有效率为96.4%,显著高于传统藻酸盐敷料组(78.2%);
再上皮化时间缩短至9.3±2.1天(对照组为15.6±3.4天);
组织病理显示胶原纤维排列有序,血管密度增加。
3.3 临床应用指南
适应症:糖尿病足溃疡(Wagner 1-3级)、Ⅱ-Ⅳ度褥疮、静脉性溃疡等慢性创面;
使用方法:清创后均匀涂抹敷料(厚度2-3mm),完全覆盖创面,每日1-2次;
联合治疗:可配合负压伤口疗法(NPWT)或高压氧治疗,以增强疗效。
3.4 指南与共识推荐
基于其明确的机制和确切的疗效,喜福永敷料已被《促进糖尿病患者足溃疡愈合的干预措施指南(2023年更新版)》和《全球糖尿病患者足溃疡治疗指南》推荐为肉芽形成期与上皮形成期慢性创面修复的主要手段之一。同时,它也被纳入《糖尿病足溃疡创面治疗专家共识(2024)》,成为“糖足”治疗的新策略。
4 与传统敷料的比较优势
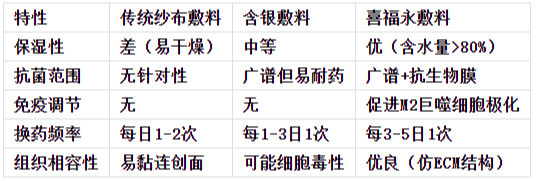
5 总结
喜福永医用伤口护理功能敷料通过复合水凝胶技术整合了湿性愈合、免疫调节、抗菌抗氧化等多重功能,直击慢性创面微环境失衡的核心问题。临床数据证实其在糖尿病足与褥疮治疗中能显著促进肉芽生长、控制感染并降低复发率。未来研究方向包括:
个性化精准治疗:基于创面生物标志物(如pH、MMP水平)开发智能响应型水凝胶,实现药物按需释放;
联合基因治疗:利用水凝胶递送siRNA或miRNA,调控创面愈合关键基因表达;
诊疗一体化:集成微传感器实时监测创面温度、pH值,动态调整治疗策略。
复合水凝胶敷料有望成为慢性创面管理从“被动覆盖”转向“主动调控”的重要工具,为患者提供更高效、经济的解决方案。
参考文献
专利:CN202110309401.7 一种用于糖尿病足伤口敷料的复合水凝胶及其制备方法。
Zhou Z, et al. Biomaterials. 2023;299:122141 (AFG/GelMA水凝胶通过巨噬细胞极化促进糖尿病伤口愈合)。
Xie H, et al. Biomaterials. 2024 (尿源性干细胞外泌体复合水凝胶靶向SERPINE1加速愈合)。
陈观平, 等. 功能性水凝胶敷料在糖尿病慢性伤口中的应用研究进展. 大连大学学报, 2024。
Shen J, et al. Adv Mater. 2023 (自级联葡萄糖耗竭与ROS清除水凝胶)。
临床医用敷料选择指南. 2023。
伤口敷料的特点与临床应用. 2023。
林瑞萍. 伤口敷料介绍与护理应用. 台北荣总医院专家讲座。